Chitosan für die Impfstoffentwicklung gegen SARS-CoV-2
Die weltweite Verbreitung des SARS-CoV-2 kann nur durch die Entwicklung von Impfstoffen eingedämmt werden. Vektor-Impfstoffe (DNA und virale) können mit den heutigen Synthesetechnologien schnell und kostengünstig hergestellt werden. Herausforderungen bei DNA-Vakzinen ist die Degradation durch DNasen, die ineffiziente Aufnahme durch Antigen-präsentierende Zellen (APC) und die geringe Immunogenität. Das partikuläre Adjuvantsystem, mit Quil-A beladene Chitosan Nanopartikel (QAC), ermöglicht den Transport der Plasmid-DNA direkt zu den Zielzellen und die Freisetzung über die Zeit. Wir stellen Ihnen hier zwei Studien zum Potential von Chitosan in der Impfstoffentwicklung vor.
Lokalisierte und systemische Immunantworten gegen SARS-CoV-2 nach mukosaler Immunisierung
Localized and Systemic Immune Responses against SARS-CoV-2 Following Mucosal Immunization. Chandrasekar, S.S.; Phanse, Y.; Hildebrand, R.E.; Hanafy, M.;Wu, C.-W.; Hansen, C.H.; Osorio, J.E.; Suresh, M.; Talaat, A.M., Vaccines 2021, 9, 132. https://doi.org/10.3390/vaccines9020132
Die Autoren hatten bereits in einer früheren Studie mit Quil-A-beladenen Chitosan (QAC)-Nanopartikel in Kombination mit Plasmidimpfstoffen gegen das Vogel-Coronavirus untersucht und eine robuste Immunantwort zeigen können. In der vorgestellten Studie wurde die Immunantwort gegenüber einer mukosalen homologen Plasmid- und einer heterologen Immunisierungsstrategie bei Verwendung eines Plasmid-Impfstoffs und des modifizierten Vakzines Ankara (MVA), welcher SARS-CoV-2 Spike (S)- und Nukleokapsid (N)-Antigene exprimiert, in Mäusen untersucht. Das Modified-Vaccinia-Ankara-Virus (MVA) ist ein abgeschwächtes Kuhpockenvirus, welches als viraler Vektor eingesetzt wird. Die effiziente Produktion im großen Maßstab ist bereits möglich und könnte zur Bekämpfung der COVID-19 Pandemie genutzt werden. Die Autoren vermuten, dass eine Kombination aus einer 1. Impfung mit der QAC-verkapselten Plasmid-DNA (Primer) und einer 2. Impfung mit einem MVA-Boost eine breiter Immunantwort auslöst (heterologe Strategie).
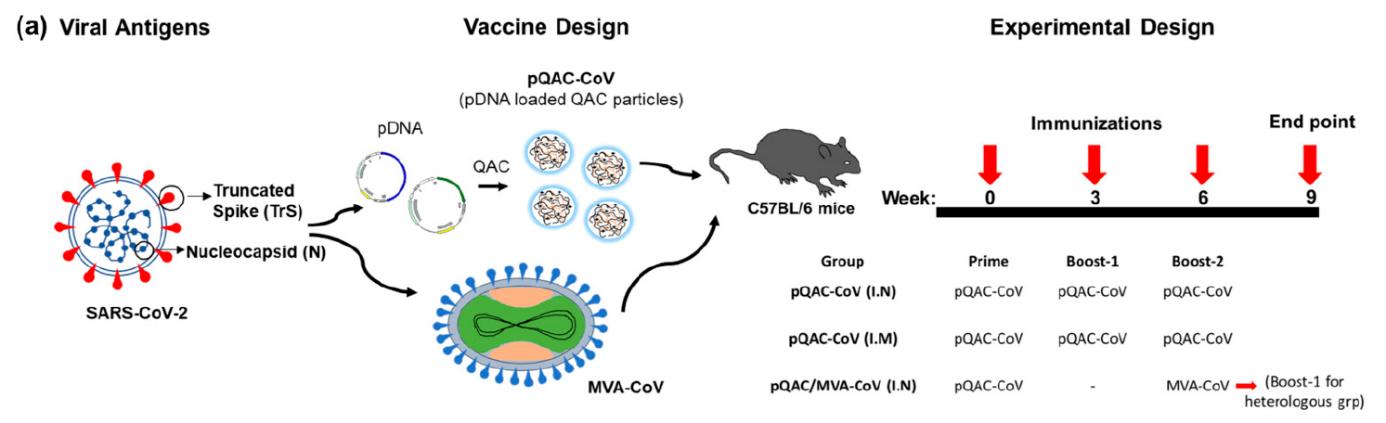
Abbildung 1: Virale Antigene, Vakzin Design und Versuchsplanung. Quelle: Localized and Systemic Immune Responses against SARS-CoV-2 Following Mucosal Immunization. Chandrasekar, S.S.; Phanse, Y.; Hildebrand, R.E.; Hanafy, M.;Wu, C.-W.; Hansen, C.H.; Osorio, J.E.; Suresh, M.; Talaat, A.M., Vaccines 2021, 9, 132. https://doi.org/10.3390/vaccines9020132
Ergebnisse
- Neutralisierende Antikörper im Serum und in der bronchoalveolären Lavage von Mäusen nur bei der heterologen intranasalen Immunsierungsstrategie
- Induktion von Typ-1 und Typ-17-T-Zell-Antworten
- Induktion von Typ-17-T-Zell Antworten (Expression von Typ-1-Zytokinen) in Lunge und Milz
- Die homologe Plasmid-Impfstrategie induzierte die Induktion von lokalen mono- und polyfunktionalen T-Zellen, welche IFN-γ sezernieren
Schlussfolgerung: Die Studienergebnisse unterstreichen das Potential der QAC-Nano-Impfstoffe, die eine Immunantwort gegenüber dem neuartigen Coronavirus hervorrufen. Die heterologe Impfstrategie scheint für die Erzeugung der Immunität besser geeignet zu sein. Die homologe Impfstrategie könnte eine SARS-CoV-2 Infektion wahrscheinlich nicht verhindern, jedoch vermutlich einen schweren Verlauf. Weiter Studien sind notwendig, um die Wirksamkeit und das Potential der Plasmid-DNA beladenen Quil-A-Chitosan Nanopartikel abschließend zu beurteilen.
Quelle: https://pubmed.ncbi.nlm.nih.gov/33562141/
In vitro Charakterisierung von inhalierbaren kationischen Hybrid-Nanopartikeln als potentielle Vakzine Träger
In Vitro Characterization of Inhalable Cationic Hybrid Nanoparticles as Potential Vaccine Carriers. Alfagih, I.M.; Kaneko, K.; Kunda, N.K.; Alanazi, F.; Dennison, S.R.; Tawfeek, H.M.; Saleem, I.Y. Pharmaceuticals 2021, 14, 164. https://doi.org/10.3390/ph14020164
Durchführung von Impfungen über die Lunge würde den natürlichen Infektionsweg von pulmonalen Erregern nachahmen und könnte dadurch eine lokale Immunantwort auslösen. Die Lunge bietet Antigen-präsentierende Zellen, wie dendritische Zellen, und eine große Oberfläche für die Absorption von Medikamenten. Zur pulmonalen Impfstoffverabreichung braucht es geeignete Formulierungen die geeignete Verabreichbarkeit, Biokompatibilität und Immunogenität bieten. Nanopartikel aus Poly(glycerinadipat-co-ω-pentadecalacton) (PGAco- PDL) könnten als Transportvehikel dienen.
Die Autoren stellten mit Rinderserumalbumin (BSA) gefüllte PGA-co-PDL-Nanopartikel (NPs) mittels Verdampfung des Emulsionslösungsmittels her. Zusätzlich wurde Chitosan Hydrochlorid (HCL) in die äußere Phase zur Oberflächenabsorption an den Nanopartikeln eingebracht. Die BSA-befüllten, kationischen Chitosan HCl Nanopartikel wurden in Nanokomposit-Mikroträger (NCMPs) aus L-Leucin eingebracht und sprühgetrocknet. Die Chitosan HCl NPs/NCMPs wurden in verschiedenen Assays bezüglich in-vitro-Aerosolisierung, Freisetzung, Zellviabilität und Aufnahme durch die Zellen sowie Proteinstrukturstabilität untersucht. Die Autoren setzten Chitosan HCl mit einem Deacetylierungsgrad von 80-95% und einem Molekulargewicht im Bereich von 200 bis 400 kDa von Heppe Medical Chitosan ein.
Ergebnisse
- Erfolgreiche Herstellung von hybriden kationischen Chitosan HCl NPs mit Partikelgrößen von 480,2±32.2 nm, einer Ladung von +14,2±0,72 mV und einer Beladung mit BSA von 7,28±1,3 µg/mg
- Bildung feiner Partikelfraktionen
- Stabile BSA-Proteinstruktur nach Freisetzung aus den Chitosan HCl NPs/NCMPs
- Nahezu vollständige Freisetzung nach 48h
- Zellviabilität von 70% bei dendritischen Zellen und A549 Zellen bei einer Konzentration von 2,5 mg/ml nach 4-24h Exposition (MTT Assay)
- Aufnahme der Chitosan HCl NPs durch die dendritischen Zellen innerhalb einer Stunde
- Aktivierung von dendritischen Zellen durch die Chitosan HCl NPs (Expression von CD40, CD86 und MHC-II-Zelloberflächenmarkern)
Schlussfolgerung: Die Studienergebnisse zeigen das Potential der Chitosan HCl NPs/NCMPs-Plattform für den Transport und die Freisetzung von Proteinen in der Lunge für immunstimulierende Anwendungen wie Impfstoffe. Die mehrschichtige Oberflächenadsorption des Chitosan HCls ermöglicht die Herstellung von positiv geladenen Nanopartikeln. Weitere Studien sind notwendig, um das Wirkstofffreisetzungssystem im Tiermodel zu testen.